Iloperidone (fanapt) Informasi Peresepan Lengkap
Nama Merek: Fanapt
Nama Generik: Iloperidone
Panduan Peresepan Fanapt (Iloperidone) (PDF)
Isi:
Peringatan Kotak
Indikasi dan Penggunaan
Dosis dan Administrasi
Kontraindikasi
Peringatan dan pencegahan
Reaksi yang merugikan
Interaksi obat
Gunakan dalam Populasi Tertentu
Penyalahgunaan dan Ketergantungan Narkoba
Overdosis
Deskripsi
Farmakologi Klinis
Toksikologi Nonklinis
Studi Klinis
Bagaimana Disediakan
Panduan Obat Brintellix
PERINGATAN: MENINGKATKAN KEMATIAN PADA PASIEN LANJUTAN DENGAN PSIKOSIS DEMENSIA-TERKAIT
Pasien lanjut usia dengan psikosis terkait demensia yang diobati dengan obat antipsikotik berisiko lebih tinggi untuk meninggal. FANAPT tidak disetujui untuk perawatan pasien dengan psikosis terkait demensia.
Indikasi dan Penggunaan
FANAPT® diindikasikan untuk pengobatan skizofrenia pada orang dewasa.
Ketika memutuskan di antara pengobatan alternatif yang tersedia untuk kondisi ini, prescriber harus mempertimbangkan temuan bahwa FANAPT dikaitkan dengan perpanjangan interval QTc. Perpanjangan interval QTc dikaitkan dalam beberapa obat lain dengan kemampuan untuk menyebabkan torsade de pointhy-type arrhythmia, sebuah takikardia ventrikel polimorfik yang berpotensi fatal yang dapat mengakibatkan tiba-tiba kematian. Dalam banyak kasus ini akan mengarah pada kesimpulan bahwa obat lain harus dicoba terlebih dahulu. Apakah FANAPT akan menyebabkan torsade de pointes atau meningkatkan laju kematian mendadak belum diketahui.
Pasien harus dititrasi ke dosis FANAPT yang efektif. Dengan demikian, pengendalian gejala mungkin tertunda selama 1 hingga 2 minggu pertama pengobatan dibandingkan dengan beberapa obat antipsikotik lain yang tidak memerlukan titrasi yang serupa. Para pemberi resep harus memperhatikan keterlambatan ini ketika memilih obat antipsikotik untuk pengobatan skizofrenia.
lanjutkan cerita di bawah ini
Dosis dan Administrasi
Dosis yang Biasa
FANAPT harus dititrasi secara perlahan dari dosis awal yang rendah untuk menghindari hipotensi ortostatik karena sifat pemblokiran alfa-adrenergiknya. Dosis awal yang disarankan untuk tablet FANAPT adalah 1 mg per oral dua kali sehari. Peningkatan dosis untuk mencapai kisaran target 6 -12 mg dua kali sehari (12_24 mg / hari) dapat dilakukan dengan penyesuaian dosis harian tidak melebihi 2 mg dua kali sehari (4 mg / hari). Dosis maksimum yang disarankan adalah 12 mg dua kali sehari (24 mg / hari). Dosis FANAPT di atas 24 mg / hari belum dievaluasi secara sistematis dalam uji klinis. Kemanjuran ditunjukkan dengan FANAPT dalam kisaran dosis 6 hingga 12 mg dua kali sehari. Para pemberi resep harus memperhatikan fakta bahwa pasien perlu dititrasi ke dosis FANAPT yang efektif. Dengan demikian, pengendalian gejala mungkin tertunda selama 1 hingga 2 minggu pertama pengobatan dibandingkan dengan beberapa obat antipsikotik lain yang tidak memerlukan titrasi yang serupa. Para pemberi resep juga harus menyadari bahwa beberapa efek buruk yang terkait dengan penggunaan FANAPT terkait dengan dosis. FANAPT dapat diberikan tanpa memperhatikan makanan.
Dosis pada Populasi Khusus
Penyesuaian dosis untuk pasien yang menggunakan FANAPT bersamaan dengan penghambat CYP2D6 potensial: Dosis FANAPT harus berkurang setengahnya ketika diberikan bersamaan dengan inhibitor CYP2D6 yang kuat seperti fluoxetine atau paroxetine. Ketika inhibitor CYP2D6 ditarik dari terapi kombinasi, dosis FANAPT kemudian harus ditingkatkan ke tempat sebelumnya.
Penyesuaian dosis untuk pasien yang menggunakan FANAPT bersamaan dengan penghambat CYP3A4 potensial: Dosis FANAPT harus dikurangi setengahnya ketika diberikan bersamaan dengan inhibitor CYP3A4 yang kuat seperti ketoconazole atau klaritromisin. Ketika inhibitor CYP3A4 ditarik dari terapi kombinasi, dosis FANAPT harus ditingkatkan ke tempat sebelumnya.
Penyesuaian dosis untuk pasien yang menggunakan FANAPT yang merupakan metabolizer CYP2D6 yang buruk: Dosis FANAPT harus dikurangi setengahnya untuk metabolizer CYP2D6 yang buruk.
Gangguan hati: Tidak ada penyesuaian dosis untuk FANAPT diperlukan pada pasien dengan gangguan hati ringan. Pasien dengan gangguan hati sedang mungkin memerlukan pengurangan dosis, jika diindikasikan secara klinis. FANAPT tidak direkomendasikan untuk pasien dengan gangguan hati berat.
Perawatan Perawatan
Dalam studi jangka panjang, FANAPT efektif dalam menunda waktu untuk kambuh pada pasien dengan skizofrenia yang distabilkan pada FANAPT hingga 24 mg / hari. Pasien harus ditinjau ulang secara berkala untuk menentukan kebutuhan perawatan perawatan.
Reinisiasi Pengobatan pada Pasien yang Sebelumnya Dihentikan Meskipun tidak ada data untuk secara spesifik menangani reinisiasi pengobatan, direkomendasikan bahwa jadwal titrasi inisiasi diikuti setiap kali pasien memiliki interval off FANAPT lebih dari 3 hari.
teratas
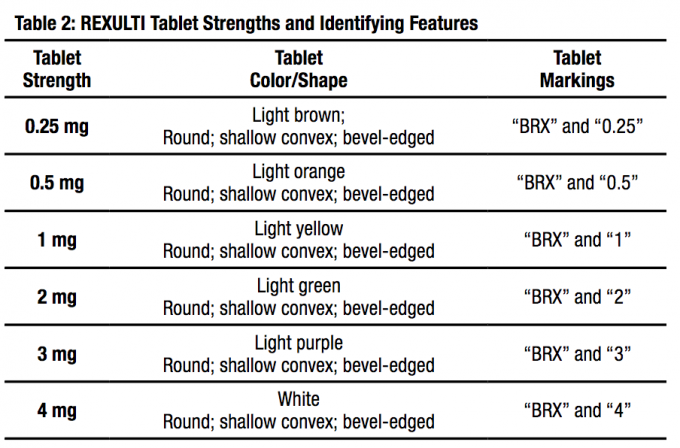
Bentuk dan kekuatan sediaan
Tablet FANAPT tersedia dalam kekuatan berikut: 1 mg, 2 mg, 4 mg, 6 mg, 8 mg, 10 mg, dan 12 mg. Tablet-tablet itu berwarna putih, bulat, pipih, bermata miring dan diidentifikasi dengan logo "" diikat di satu sisi dan kekuatan tablet "1", "2", "4", "6", "8", "8", "10", atau "12" debossed di sisi lain.
teratas
Kontraindikasi
FANAPT dikontraindikasikan pada individu dengan reaksi hipersensitif terhadap produk. Anafilaksis, angioedema, dan reaksi hipersensitivitas lainnya telah dilaporkan.
teratas
PERINGATAN DAN PENCEGAHAN
Peningkatan Mortalitas pada Pasien Lansia dengan Psikosis Terkait Demensia
Obat antipsikotik meningkatkan risiko kematian semua penyebab pada pasien usia lanjut dengan psikosis terkait demensia. Menganalisis 17 uji coba terkontrol plasebo terkait psikosis terkait demensia (durasi modal 10 minggu dan sebagian besar pada pasien yang menggunakan atipikal obat antipsikotik) mengungkapkan risiko kematian pada pasien yang diobati dengan obat antara 1,6 hingga 1,7 kali pada pasien yang diobati dengan plasebo. Selama uji coba terkontrol 10 minggu, tingkat kematian pada pasien yang diobati dengan obat adalah sekitar 4,5%, dibandingkan dengan tingkat sekitar 2,6% pada pasien yang diobati dengan plasebo.
Meskipun penyebab kematian bervariasi, sebagian besar kematian tampaknya bersifat kardiovaskular (mis., Gagal jantung, kematian mendadak) atau menular (mis., Pneumonia) di alam. FANAPT tidak disetujui untuk perawatan pasien dengan psikosis terkait demensia.
Efek Samping Serebrovaskular, Termasuk Stroke, pada Pasien Lansia dengan Psikosis Terkait Demensia
Dalam uji coba terkontrol plasebo pada subjek manula dengan demensia, pasien diacak untuk risperidone, aripiprazole, dan olanzapine memiliki insiden stroke dan serangan iskemik transien yang lebih tinggi, termasuk fatal pukulan. FANAPT tidak disetujui untuk perawatan pasien dengan psikosis terkait demensia.
Perpanjangan QT
Dalam studi label terbuka QTc pada pasien dengan skizofrenia atau gangguan schizoafektif (n = 160), FANAPT dikaitkan dengan perpanjangan QTc 9 msec dengan dosis iloperidone 12 mg dua kali sehari. Efek FANAPT pada interval QT ditambah dengan adanya penghambatan metabolisme CYP450 2D6 atau 3A4 (paroxetine 20 mg sehari sekali dan ketoconazole 200 mg dua kali sehari, masing-masing). Dalam kondisi penghambatan metabolisme untuk 2D6 dan 3A4, FANAPT 12 mg dua kali sehari dikaitkan dengan peningkatan QTcF rata-rata dari awal sekitar 19 msec.
Tidak ada kasus torsade de pointes atau aritmia jantung berat lainnya yang diamati selama program klinis pra-pemasaran.
Penggunaan FANAPT harus dihindari dalam kombinasi dengan obat lain yang diketahui memperpanjang QTc termasuk Kelas 1A (mis., Quinidine, procainamide) atau Kelas III (mis., amiodarone, sotalol) obat antiaritmia, obat antipsikotik (mis., chlorpromazine, thioridazine), antibiotik (mis., gatifloksasin, moksifloksasin), atau golongan obat lain apa pun yang diketahui memperpanjang interval QTc (mis., pentamidin, levomethadyl asetat, metadon). FANAPT juga harus dihindari pada pasien dengan sindrom QT bawaan panjang dan pada pasien dengan riwayat aritmia jantung.
Keadaan tertentu dapat meningkatkan risiko torsade de pointes dan / atau kematian mendadak sehubungan dengan penggunaan obat yang memperpanjang interval QTc, termasuk (1) bradikardia; (2) hipokalemia atau hipomagnesemia; (3) penggunaan obat lain secara bersamaan yang memperpanjang interval QTc; dan (4) adanya perpanjangan bawaan dari interval QT; (5) infark miokard akut baru-baru ini; dan / atau (6) gagal jantung tidak terkompensasi.
Perhatian diperlukan saat meresepkan FANAPT dengan obat yang menghambat metabolisme FANAPT, dan pada pasien dengan berkurangnya aktivitas CYP2D6.
Dianjurkan agar pasien dipertimbangkan untuk perawatan FANAPT yang berisiko signifikan gangguan elektrolit memiliki pengukuran kalium dan magnesium serum awal dengan periodik pemantauan. Hipokalemia (dan / atau hipomagnesemia) dapat meningkatkan risiko perpanjangan QT dan aritmia. FANAPT harus dihindari pada pasien dengan riwayat penyakit kardiovaskular yang signifikan, misalnya QT perpanjangan, infark miokard akut baru-baru ini, gagal jantung tak terkompensasi, atau aritmia jantung. FANAPT harus dihentikan pada pasien yang ditemukan memiliki pengukuran QTc persisten> 500 msec.
Jika pasien yang menggunakan FANAPT mengalami gejala yang dapat menunjukkan terjadinya aritmia jantung, mis., pusing, palpitasi, atau sinkop, resep harus memulai evaluasi lebih lanjut, termasuk jantung pemantauan.
Neuroleptic Malignant Syndrome (NMS)
Kompleks gejala yang berpotensi fatal kadang-kadang disebut sebagai Neuroleptic Malignant Syndrome (NMS) telah dilaporkan berkaitan dengan pemberian obat antipsikotik, termasuk FANAPT. Manifestasi klinis termasuk hiperpireksia, kekakuan otot, perubahan status mental (termasuk tanda katatonik) dan bukti ketidakstabilan otonom (denyut nadi atau tekanan darah tidak teratur, takikardia, diaforesis, dan jantung) disritmia). Tanda-tanda tambahan mungkin termasuk peningkatan kreatin fosfokinase, mioglobinuria (rhabdomyolysis), dan gagal ginjal akut. Evaluasi diagnostik pasien dengan sindrom ini rumit. Dalam mencapai suatu diagnosis, penting untuk mengidentifikasi kasus-kasus yang termasuk dalam presentasi klinis baik penyakit medis serius dan tanda-tanda dan gejala ekstrapiramidal yang tidak diobati atau tidak diobati (EPS). Pertimbangan penting lainnya dalam diagnosis diferensial termasuk toksisitas antikolinergik sentral, stroke panas, demam obat, dan patologi sistem saraf pusat primer (SSP).
Penatalaksanaan sindrom ini harus meliputi: (1) penghentian segera obat-obatan antipsikotik dan obat-obatan lain yang tidak penting untuk terapi bersamaan, (2) perawatan simtomatik intensif dan pemantauan medis, dan (3) perawatan dari setiap masalah medis serius yang bersamaan dengan perawatan spesifik yang tersedia. Tidak ada kesepakatan umum tentang rejimen pengobatan farmakologis spesifik untuk NMS.
Jika seorang pasien memerlukan perawatan obat antipsikotik setelah pemulihan dari NMS, potensi reintroduksi terapi obat harus dipertimbangkan dengan cermat. Pasien harus dimonitor dengan hati-hati, karena kekambuhan NMS telah dilaporkan.
Diskinesia Tardive
Tardive dyskinesia adalah suatu sindrom yang terdiri dari gerakan-gerakan diskinetik yang mungkin tidak dapat dipulihkan, tidak disengaja, yang dapat berkembang pada pasien-pasien yang diobati dengan obat-obatan antipsikotik. Meskipun prevalensi sindrom tampaknya paling tinggi di antara orang tua, terutama wanita lanjut usia, tidak mungkin mengandalkan perkiraan prevalensi untuk memprediksi, pada permulaan pengobatan antipsikotik, yang cenderung dikembangkan oleh pasien sindroma. Apakah produk obat antipsikotik berbeda dalam potensinya untuk menyebabkan tardive dyskinesia tidak diketahui.
Risiko mengembangkan tardive dyskinesia dan kemungkinan hal itu akan menjadi ireversibel diyakini meningkat seiring lamanya pengobatan dan dosis kumulatif total antipsikotik yang diberikan meningkat. Namun, sindrom ini dapat berkembang, walaupun jauh lebih jarang, setelah periode perawatan yang relatif singkat dengan dosis rendah.
Tidak ada pengobatan yang diketahui untuk kasus-kasus tardive dyskinesia yang telah mapan, walaupun sindrom ini dapat sembuh, sebagian atau seluruhnya, jika pengobatan antipsikotik dihentikan. Namun, pengobatan antipsikotik itu sendiri dapat menekan (atau menekan sebagian) tanda-tanda dan gejala-gejala sindrom tersebut dan dengan demikian mungkin menutupi proses yang mendasarinya. Efek dari penindasan simptomatik terhadap sindrom jangka panjang tidak diketahui.
Dengan pertimbangan ini, FANAPT harus diresepkan dengan cara yang paling mungkin untuk meminimalkan terjadinya tardive dyskinesia. Perawatan antipsikotik kronis umumnya harus disediakan untuk pasien yang menderita penyakit kronis yang (1) diketahui merespons obat antipsikotik, dan (2) untuk siapa alternatif, sama-sama efektif, tetapi pengobatan yang berpotensi kurang berbahaya tidak tersedia atau sesuai. Pada pasien yang memerlukan perawatan kronis, dosis terkecil dan durasi perawatan terpendek yang menghasilkan respon klinis yang memuaskan harus dicari. Kebutuhan akan perawatan lanjutan harus dinilai kembali secara berkala.
Jika tanda dan gejala tardive dyskinesia muncul pada pasien dengan FANAPT, penghentian obat harus dipertimbangkan. Namun, beberapa pasien mungkin memerlukan pengobatan dengan FANAPT meskipun ada sindrom.
Perubahan Metabolik
Obat antipsikotik atipikal telah dikaitkan dengan perubahan metabolisme yang dapat meningkatkan risiko kardiovaskular / serebrovaskular. Perubahan metabolisme ini termasuk hiperglikemia, dislipidemia, dan pertambahan berat badan. Sementara semua obat antipsikotik atipikal telah terbukti menghasilkan beberapa perubahan metabolisme, masing-masing obat di kelas memiliki profil risiko spesifik.
Hiperglikemia dan Diabetes Mellitus
Hiperglikemia, dalam beberapa kasus ekstrem dan berhubungan dengan ketoasidosis atau koma atau kematian hiperosmolar, telah dilaporkan pada pasien yang diobati dengan antipsikotik atipikal termasuk FANAPT. Penilaian hubungan antara penggunaan antipsikotik atipikal dan kelainan glukosa dipersulit oleh kemungkinan peningkatan latar belakang risiko diabetes mellitus pada pasien dengan skizofrenia dan meningkatnya kejadian diabetes mellitus secara umum populasi. Mengingat perancu ini, hubungan antara penggunaan antipsikotik atipikal dan efek samping terkait hiperglikemia tidak sepenuhnya dipahami. Namun, studi epidemiologis menunjukkan peningkatan risiko efek samping terkait hiperglikemia pada pasien yang diobati dengan antipsikotik atipikal yang termasuk dalam studi ini.
Pasien dengan diagnosis diabetes mellitus yang dimulai dengan antipsikotik atipikal harus dipantau secara teratur untuk memperburuk kontrol glukosa. Pasien dengan faktor risiko diabetes mellitus (mis., Obesitas, riwayat keluarga diabetes) yang memulai pengobatan antipsikotik atipikal harus menjalani tes glukosa darah puasa pada awal pengobatan dan secara berkala selama pengobatan. Setiap pasien yang diobati dengan antipsikotik atipikal harus dipantau untuk gejala hiperglikemia termasuk polydipsia, poliuria, polifagia, dan kelemahan. Pasien yang mengalami gejala hiperglikemia selama pengobatan dengan antipsikotik atipikal harus menjalani tes glukosa darah puasa. Dalam beberapa kasus, hiperglikemia telah sembuh ketika antipsikotik atipikal dihentikan; Namun, beberapa pasien memerlukan kelanjutan pengobatan antidiabetik meskipun penghentian obat yang dicurigai.
Data dari studi 4 minggu, dosis tetap pada subjek dewasa dengan skizofrenia, di mana sampel darah puasa diambil, disajikan pada Tabel 1.
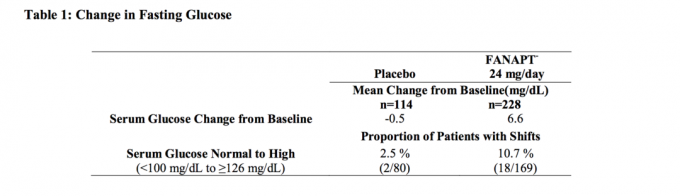
Analisis yang dikumpulkan dari data glukosa dari studi klinis termasuk uji coba jangka panjang ditunjukkan pada Tabel2.
Dislipidemia
Perubahan yang tidak diinginkan pada lipid telah diamati pada pasien yang diobati dengan antipsikotik atipikal.
Data dari kelompok yang dikendalikan plasebo, 4 minggu, dosis tetap, di mana sampel darah puasa diambil, pada subjek dewasa dengan skizofrenia disajikan pada Tabel 3.

Analisis gabungan dari data kolesterol dan trigliserida dari studi klinis termasuk uji coba jangka panjang ditunjukkan pada Tabel 4 dan Tabel 5.
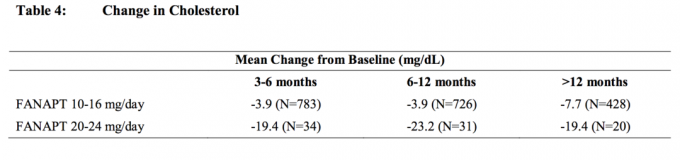
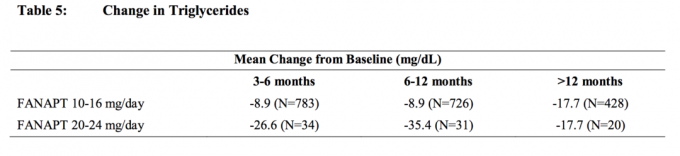
Berat badan
Peningkatan berat badan telah diamati dengan penggunaan antipsikotik atipikal. Pemantauan klinis berat direkomendasikan.
Di semua studi jangka pendek dan jangka panjang, perubahan rata-rata keseluruhan dari awal pada titik akhir adalah 2,1 kg.
Perubahan berat badan (kg) dan proporsi subjek dengan ≥7% kenaikan berat badan dari 4 studi yang dikontrol plasebo, 4- atau 6 minggu, dosis tetap atau fleksibel pada subyek dewasa disajikan di Tabel 6.
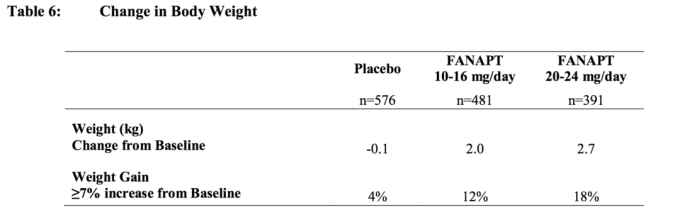
Kejang
Dalam uji coba terkontrol plasebo jangka pendek (4-6 minggu), kejang terjadi pada 0,1% (1/1344) pasien yang diobati dengan FANAPT dibandingkan dengan 0,3% (2/587) pada plasebo. Seperti halnya antipsikotik lainnya, FANAPT harus digunakan dengan hati-hati pada pasien dengan riwayat kejang atau dengan kondisi yang berpotensi menurunkan ambang kejang. Kondisi yang menurunkan ambang kejang mungkin lebih umum pada populasi 65 tahun atau lebih.
Hipotensi dan Sinkronisasi ortostatik
FANAPT dapat menyebabkan hipotensi ortostatik yang terkait dengan pusing, takikardia, dan sinkop. Ini mencerminkan sifat antagonis alfa1-adrenergiknya. Dalam studi jangka pendek terkontrol plasebo double-blind, di mana dosis ditingkatkan perlahan, seperti yang direkomendasikan di atas, sinkop dilaporkan pada 0,4% (5/1344) pasien yang diobati dengan FANAPT, dibandingkan dengan 0,2% (1/587) pada plasebo. Hipotensi ortostatik dilaporkan pada 5% pasien yang diberi 20-24 mg / hari, 3% pasien diberi 10-16 mg / hari, dan 1% pasien diberi plasebo. Titrasi yang lebih cepat diharapkan akan meningkatkan laju hipotensi ortostatik dan sinkop.
FANAPT harus digunakan dengan hati-hati pada pasien dengan penyakit kardiovaskular yang diketahui (misalnya, gagal jantung, riwayat infark miokard, iskemia, atau konduksi). kelainan), penyakit serebrovaskular, atau kondisi yang membuat pasien rentan terhadap hipotensi (dehidrasi, hipovolemia, dan pengobatan dengan antihipertensi). obat-obatan). Pemantauan tanda-tanda vital ortostatik harus dipertimbangkan pada pasien yang rentan terhadap hipotensi.
Leukopenia, Neutropenia dan Agranulocytosis
Dalam pengalaman uji klinis dan pasca pemasaran, kejadian leukopenia / neutropenia telah dilaporkan sementara terkait dengan agen antipsikotik. Agranulositosis (termasuk kasus fatal) juga telah dilaporkan.
Faktor-faktor risiko yang mungkin untuk leukopenia / neutropenia termasuk jumlah sel darah putih (WBC) yang sudah ada sebelumnya dan riwayat leukopenia / neutropenia yang diinduksi obat. Pasien dengan WBC rendah yang sudah ada sebelumnya atau riwayat leukopenia / neutropenia yang diinduksi obat harus dipantau hitung darah lengkapnya (CBC). sering selama beberapa bulan pertama terapi dan harus menghentikan FANAPT pada tanda pertama dari penurunan WBC tanpa adanya penyebab lain faktor.
Pasien dengan neutropenia harus dimonitor dengan hati-hati untuk demam atau gejala atau tanda infeksi lain dan segera diobati jika gejala atau tanda tersebut muncul. Pasien dengan neutropenia berat (jumlah neutrofil absolut <1000 / mm3) harus menghentikan FANAPT dan menjalani WBC hingga pemulihan.
Hiperprolaktinemia
Seperti halnya obat lain yang memusuhi reseptor D2 dopamin, FANAPT meningkatkan kadar prolaktin.
Hiperprolaktinemia dapat menekan GnRH hipotalamus, sehingga mengurangi sekresi gonadotropin hipofisis. Hal ini, pada gilirannya, dapat menghambat fungsi reproduksi dengan merusak gonadosteroidogenesis pada pasien wanita dan pria. Galaktorea, amenorea, ginekomastia, dan impotensi telah dilaporkan dengan senyawa yang meningkatkan prolaktin. Hiperprolaktinemia jangka panjang ketika dikaitkan dengan hipogonadisme dapat menyebabkan penurunan kepadatan tulang pada pasien wanita dan pria.
Eksperimen kultur jaringan menunjukkan bahwa sekitar sepertiga kanker payudara manusia bergantung pada prolaktin in vitro, a faktor penting yang potensial jika resep obat ini direnungkan pada pasien dengan payudara yang terdeteksi sebelumnya kanker. Perubahan proliferatif kelenjar susu dan peningkatan prolaktin serum terlihat pada tikus dan tikus yang diobati dengan FANAPT. Tidak ada studi klinis maupun studi epidemiologi yang dilakukan hingga saat ini yang menunjukkan hubungan antara pemberian kronis dari kelas obat ini dan tumorigenesis pada manusia; bukti yang ada dianggap terlalu terbatas untuk menjadi konklusif saat ini.
Dalam uji coba terkontrol plasebo jangka pendek (4 minggu), perubahan rata-rata dari awal menjadi titik akhir dalam kadar prolaktin plasma untuk kelompok FANAPT 24 mg / hari yang diobati adalah peningkatan 2,6 ng / mL dibandingkan dengan penurunan 6,3 ng / mL dalam kelompok plasebo. Dalam percobaan ini, peningkatan kadar prolaktin plasma diamati pada 26% orang dewasa yang diobati dengan FANAPT dibandingkan dengan 12% pada kelompok plasebo. Dalam uji coba jangka pendek, FANAPT dikaitkan dengan tingkat sederhana dari peningkatan prolaktin dibandingkan dengan peningkatan prolaktin yang lebih besar yang diamati dengan beberapa agen antipsikotik lainnya. Dalam analisis gabungan dari studi klinis termasuk uji coba jangka panjang, pada 3.210 orang dewasa yang diobati dengan iloperidone, ginekomastia dilaporkan dalam 2 subjek laki-laki (0,1%) dibandingkan dengan 0% pada pasien yang diobati dengan plasebo, dan galaktorea dilaporkan pada 8 subjek wanita (0,2%) dibandingkan dengan 3 subjek wanita (0,5%) pada pasien yang diobati dengan plasebo pasien.
Pengaturan Suhu Tubuh
Gangguan kemampuan tubuh untuk mengurangi suhu tubuh inti telah dikaitkan dengan agen antipsikotik. Perawatan yang tepat disarankan ketika meresepkan FANAPT untuk pasien yang akan mengalami kondisi yang dapat berkontribusi pada peningkatan tubuh inti. suhu, mis., berolahraga dengan keras, pajanan terhadap panas ekstrem, menerima obat yang bersamaan dengan aktivitas antikolinergik, atau menjadi sasaran dehidrasi.
Disfagia
Dismotilitas dan aspirasi kerongkongan telah dikaitkan dengan penggunaan obat antipsikotik. Pneumonia aspirasi merupakan penyebab umum morbiditas dan mortalitas pada pasien usia lanjut. FANAPT dan obat-obatan antipsikotik lainnya harus digunakan dengan hati-hati pada pasien yang berisiko mengalami pneumonia aspirasi.
Bunuh diri
Kemungkinan upaya bunuh diri melekat pada penyakit psikotik, dan pengawasan ketat terhadap pasien berisiko tinggi harus menyertai terapi obat. Resep untuk FANAPT harus ditulis untuk jumlah terkecil dari tablet yang konsisten dengan manajemen pasien yang baik untuk mengurangi risiko overdosis.
Priapisme
Tiga kasus priapisme dilaporkan dalam program FANAPT pra-pemasaran. Obat-obatan dengan efek pemblokiran alpha-adrenergik telah dilaporkan memicu priapism. FANAPT membagikan kegiatan farmakologis ini. Priapisme parah mungkin memerlukan intervensi bedah.
Potensi Gangguan Kognitif dan Motor
FANAPT, seperti antipsikotik lainnya, memiliki potensi untuk merusak penilaian, kemampuan berpikir atau motorik. Dalam jangka pendek, uji coba terkontrol plasebo, somnolen (termasuk sedasi) dilaporkan pada 11,9% (104/874) dari pasien dewasa yang diobati dengan FANAPT dengan dosis 10 mg / hari atau lebih besar dibandingkan 5,3% (31/587) yang diobati dengan plasebo. Pasien harus diperingatkan tentang pengoperasian mesin berbahaya, termasuk mobil, sampai mereka cukup yakin bahwa terapi dengan FANAPT tidak mempengaruhi mereka secara buruk.
teratas
Reaksi yang merugikan
Pengalaman Studi Klinis
Karena uji klinis dilakukan dalam kondisi yang sangat bervariasi, laju reaksi merugikan diamati dalam uji klinis obat tidak dapat secara langsung dibandingkan dengan tingkat dalam uji klinis obat lain dan mungkin tidak mencerminkan tingkat yang diamati dalam klinis praktek. Informasi di bawah ini berasal dari database uji klinis untuk FANAPT yang terdiri dari 3229 pasien yang terpapar FANAPT dengan dosis 10 mg / hari atau lebih, untuk pengobatan skizofrenia. Dari jumlah tersebut, 999 menerima FANAPT selama setidaknya 6 bulan, dengan 657 terkena FANAPT selama setidaknya 12 bulan. Semua pasien yang menerima FANAPT berpartisipasi dalam uji klinis dosis ganda. Kondisi dan lamanya pengobatan dengan FANAPT sangat bervariasi dan termasuk (dalam kategori yang tumpang tindih), label terbuka dan studi fase ganda, rawat inap dan rawat jalan, studi dosis tetap dan dosis fleksibel, dan jangka pendek dan jangka panjang paparan.
Informasi yang disajikan dalam bagian ini berasal dari kumpulan data dari 4 terkontrol plasebo, 4 atau 6 minggu, studi dosis tetap atau fleksibel pada pasien yang menerima FANAPT dengan dosis harian dalam kisaran 10 hingga 24 mg (n = 874).
Efek Samping yang Terjadi pada Insiden 2% atau Lebih di antara Pasien yang Diperlakukan FANAPT dan Lebih Sering dari pada Plasebo
Tabel 7 menyebutkan insiden reaksi merugikan yang dikumpulkan yang secara spontan dilaporkan dalam empat minggu yang dikontrol plasebo, 4 atau 6 minggu, studi dosis tetap atau fleksibel, mendaftar reaksi-reaksi yang terjadi pada 2% atau lebih dari pasien yang diobati dengan FANAPT dalam salah satu dosis kelompok, dan yang insidennya pada pasien yang diobati dengan FANAPT dalam kelompok dosis apa pun lebih besar daripada kejadian pada pasien yang diobati plasebo.
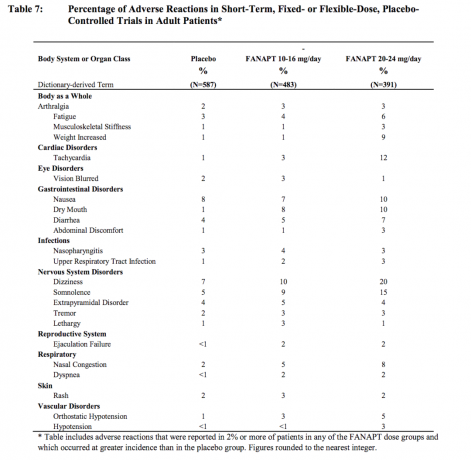
Reaksi yang merugikan terkait dosis dalam uji klinis
Berdasarkan data yang dikumpulkan dari 4 studi dengan dosis terkontrol plasebo, 4 atau 6 minggu, dosis tetap atau fleksibel, reaksi merugikan yang terjadi dengan lebih dari 2% kejadian pada pasien yang diobati dengan FANAPT, dan untuk yang kejadiannya pada pasien yang diobati dengan FANAPT 20-24 mg / hari adalah dua kali lipat dari pada pasien yang diobati dengan FANAPT 10 -16 mg / hari adalah: ketidaknyamanan perut, pusing, hipotensi, kekakuan muskuloskeletal, takikardia, dan berat badan. meningkat.
Reaksi Merugikan Umum dan Terkait Obat dalam Uji Klinis
Berdasarkan data yang dikumpulkan dari 4 studi yang dikontrol plasebo, 4 atau 6 minggu, dosis tetap atau fleksibel, reaksi merugikan berikut terjadi pada kejadian ≥5% pada pasien yang diobati. dengan FANAPT dan setidaknya dua kali plasebo tikus untuk setidaknya 1 dosis: pusing, mulut kering, kelelahan, hidung tersumbat, mengantuk, takikardia, hipotensi ortostatik, dan berat badan meningkat. Pusing, takikardia, dan peningkatan berat badan setidaknya dua kali lebih umum pada 20-24 mg / hari pada 10-16 mg / hari.
Gejala Extrapyramidal (EPS) dalam Uji Klinis
Data yang dikumpulkan dari 4 studi terkontrol plasebo, 4- atau 6- minggu, dosis tetap atau fleksibel memberikan informasi mengenai EPS. Data kejadian buruk yang dikumpulkan dari uji coba tersebut menunjukkan tingkat efek samping terkait EPS berikut seperti yang ditunjukkan pada Tabel 8.

Reaksi yang merugikan terkait dengan penghentian pengobatan dalam uji klinis
Berdasarkan data yang dikumpulkan dari 4 studi terkontrol plasebo, 4 atau 6 minggu, tetap atau fleksibel, tidak ada perbedaan dalam insiden penghentian karena efek samping antara yang diobati dengan FANAPT (5%) dan yang diobati dengan plasebo (5%) pasien. Jenis-jenis efek samping yang menyebabkan penghentian adalah serupa untuk pasien yang diobati dengan FANAPT dan plasebo.
Perbedaan Demografis dalam Reaksi yang Tidak Baik pada Uji Klinis
Pemeriksaan populasi subkelompok dalam 4 placebo-controlled, 4- atau 6 minggu, fix- atau studi dosis fleksibel tidak mengungkapkan bukti perbedaan keamanan berdasarkan usia, jenis kelamin atau ras.
Abnormalitas Uji Laboratorium dalam Uji Klinis
Tidak ada perbedaan antara FANAPT dan plasebo dalam kejadian penghentian karena perubahan hematologi, urinalisis, atau kimia serum.
Dalam uji coba terkontrol plasebo jangka pendek (4-6 minggu), terdapat 1,0% (13/1342) pasien yang diterapi iloperidon dengan hematokrit setidaknya satu kali di bawah rentang normal yang diperluas selama perawatan pasca-pengacakan, dibandingkan dengan 0,3% (2/585) pada plasebo. Kisaran normal yang diperluas untuk hematokrit yang diturunkan didefinisikan dalam masing-masing uji coba ini sebagai nilai 15% di bawah kisaran normal untuk laboratorium terpusat yang digunakan dalam uji coba.
Reaksi Lain Selama Evaluasi Pra Pemasaran FANAPT
Berikut ini adalah daftar istilah MedDRA yang mencerminkan reaksi merugikan pada pasien yang diobati dengan FANAPT pada berbagai dosis ≥ 4 mg / hari selama fase percobaan dengan database 3210 yang diobati dengan FANAPT pasien. Semua reaksi yang dilaporkan dimasukkan kecuali yang sudah tercantum dalam Tabel 7, atau bagian lain dari Reaksi Merugikan (6), yang dipertimbangkan dalam Peringatan dan Kewaspadaan (5), istilah reaksi yang begitu umum sehingga tidak informatif, reaksi dilaporkan pada kurang dari 3 pasien dan yang tidak serius atau mengancam jiwa, reaksi yang biasa terjadi sebagai reaksi latar belakang, dan reaksi yang dianggap tidak mungkin sebagai obat terkait.
Reaksi selanjutnya dikategorikan berdasarkan kelas organ sistem MedDRA dan terdaftar dalam urutan frekuensi yang menurun sesuai dengan yang berikut definisi: sering terjadi efek samping yang terjadi pada setidaknya 1/100 pasien (hanya mereka yang tidak tercantum dalam Tabel 7 yang muncul dalam hal ini) daftar); efek samping yang jarang terjadi adalah yang terjadi pada 1/100 hingga 1/1000 pasien; kejadian langka adalah yang terjadi pada kurang dari 1/1000 pasien.
Gangguan Darah dan Limfatik: Jarang- anemia, anemia defisiensi besi; Jarang-leukopenia
Gangguan Jantung: Sering - palpitasi; Jarang - aritmia, blok atrioventrikular derajat pertama, gagal jantung (termasuk kongestif dan akut)
Gangguan Telinga dan Labirin: Jarang –vertigo, tinitus
Gangguan Endokrin: Jarang- hipotiroidisme
Gangguan Mata: Sering - konjungtivitis (termasuk alergi); Jarang - mata kering, blepharitis, edema kelopak mata, pembengkakan mata, kekeruhan lenticular, katarak, hiperemia (termasuk konjungtiva)
Gangguan Gastrointestinal: Jarang - gastritis, hipersekresi saliva, inkontinensia fekal, ulserasi mulut; Stomatitis aphthous, ulkus duodenum, hiatus hernia, hiperklorhidria, ulserasi bibir, refluks esofagitis, stomatitis
Gangguan Umum dan Kondisi Situs Administratif: Jarang - edema (umum, pitting, karena penyakit jantung), kesulitan berjalan, haus; Jarang - hipertermia
Gangguan Hepatobilier: Jarang - kolelitiasis
Investigasi: Sering: berat badan turun; Jarang - hemoglobin menurun, jumlah neutrofil meningkat, hematokrit menurun
Gangguan Metabolisme dan Gizi: Jarang - peningkatan nafsu makan, dehidrasi, hipokalemia, retensi cairan
Gangguan Jaringan Muskuloskeletal dan Konektif: Sering - mialgia, kejang otot; Jarang - torticollis
Gangguan Sistem Saraf: Jarang-paresthesia, hiperaktif psikomotor, kegelisahan, amnesia, nystagmus; Sindrom kaki yang jarang gelisah
Gangguan Jiwa: Sering - gelisah, agresi, khayalan; Jarang - permusuhan, penurunan libido, paranoia, anorgasmia, keadaan kebingungan, mania, katatonia, perubahan suasana hati, panik serangan, gangguan obsesif-kompulsif, bulimia nervosa, delirium, polidipsia psikogenik, gangguan kontrol-impuls, mayor depresi
Gangguan Ginjal dan Urin: Sering - inkontinensia urin; Jarang - disuria, pollakiuria, enuresis, nephrolithiasis; Jarang - retensi urin, gagal ginjal akut
Sistem Reproduksi dan Gangguan Payudara: Disfungsi ereksi yang sering; Jarang - nyeri testis, amenorea, nyeri payudara; Jarang - menstruasi tidak teratur, ginekomastia, menoragia, metrorrhagia, perdarahan pascamenopause, prostatitis.
Gangguan Pernafasan, Thorasik dan Mediastinum: Jarang - epistaksis, asma, rinore, hidung tersumbat, hidung kering; Langka - tenggorokan kering, sindrom apnea tidur, dispnea saat aktivitas
Pengalaman Postmarketing
Reaksi merugikan berikut telah diidentifikasi selama penggunaan FANAPT pasca persetujuan: ejakulasi mundur dan reaksi hipersensitivitas (termasuk anafilaksis; angioedema; sesak tenggorokan; pembengkakan orofaringeal; pembengkakan pada wajah, bibir, mulut, dan lidah; urtikaria; ruam; dan pruritus). Karena reaksi ini dilaporkan secara sukarela dari populasi dengan ukuran tidak pasti, tidak mungkin untuk memperkirakan frekuensi mereka dengan andal atau membangun hubungan sebab akibat dengan paparan obat.
teratas
Interaksi obat
Mengingat efek SSP utama dari FANAPT, kehati-hatian harus digunakan ketika digunakan dalam kombinasi dengan obat dan alkohol yang bekerja secara terpusat. Karena antagonisme reseptor alfa1-adrenergik, FANAPT memiliki potensi untuk meningkatkan efek agen antihipertensi tertentu.
Potensi Obat Lain untuk Mempengaruhi FANAPT
Iloperidone bukan substrat untuk CYP1A1, CYP1A2, CYP2A6, CYP2B6, CYP2C8, CYP2C9, CYP2C19, atau CYP2E1. Ini menunjukkan bahwa interaksi iloperidone dengan inhibitor atau penginduksi enzim ini, atau faktor lain, seperti merokok, tidak mungkin. Baik CYP3A4 dan CYP2D6 bertanggung jawab untuk metabolisme iloperidone. Inhibitor CYP3A4 (mis., Ketoconazole) atau CYP2D6 (mis., Fluoxetine, paroxetine) dapat menghambat eliminasi iloperidone dan menyebabkan peningkatan level darah.
Ketoconazole: Pemberian bersama ketoconazole (200 mg dua kali sehari selama 4 hari), inhibitor kuat CYP3A4, dengan iloperidone dosis tunggal 3 mg hingga 19 relawan sehat, usia 18-45 tahun, meningkatkan area di bawah kurva (AUC) iloperidone dan metabolitnya P88 dan P95 sebesar 57%, 55% dan 35%, masing-masing. Dosis Iloperidone harus dikurangi sekitar setengah ketika diberikan dengan ketoconazole atau inhibitor kuat CYP3A4 lainnya (mis., Itraconazole). Inhibitor yang lebih lemah (mis., Eritromisin, jus grapefruit) belum diteliti. Ketika inhibitor CYP3A4 ditarik dari terapi kombinasi, dosis iloperidon harus dikembalikan ke tingkat sebelumnya.
Fluoxetine: Pemberian bersama fluoxetine (20 mg dua kali sehari selama 21 hari), sebuah inhibitor kuat CYP2D6, dengan dosis tunggal iloperidone 3 mg untuk 23 sukarelawan sehat, usia 29-44 tahun, yang dikategorikan sebagai metabolizer luas CYP2D6, meningkatkan AUC iloperidone dan metabolitnya P88, sekitar 2 hingga 3 kali lipat, dan menurunkan AUC metabolitnya P95 dengan setengah. Dosis Iloperidone harus dikurangi setengahnya ketika diberikan dengan fluoxetine. Ketika fluoxetine ditarik dari terapi kombinasi, dosis iloperidone harus dikembalikan ke tingkat sebelumnya. Inhibitor kuat CYP2D6 lainnya diharapkan memiliki efek yang sama dan membutuhkan pengurangan dosis yang tepat. Ketika inhibitor CYP2D6 ditarik dari terapi kombinasi, dosis iloperidone kemudian dapat ditingkatkan ke tingkat sebelumnya.
Paroxetine: Pemberian bersama paroxetine (20 mg / hari selama 5-8 hari), inhibitor kuat CYP2D6, dengan beberapa dosis iloperidone (8 atau 12 mg dua kali sehari) untuk pasien dengan skizofrenia usia 18-65 tahun mengakibatkan peningkatan rata-rata konsentrasi puncak keadaan tunak dari iloperidone dan metabolitnya P88, sekitar 1,6 kali lipat, dan penurunan rata-rata konsentrasi puncak steady-state metabolit P95 oleh setengah. Dosis Iloperidone harus dikurangi setengahnya ketika diberikan dengan paroxetine. Ketika paroxetine ditarik dari terapi kombinasi, dosis iloperidone harus dikembalikan ke tingkat sebelumnya. Inhibitor kuat CYP2D6 lainnya diharapkan memiliki efek yang sama dan membutuhkan pengurangan dosis yang tepat. Ketika inhibitor CYP2D6 ditarik dari terapi kombinasi, dosis iloperidone kemudian dapat ditingkatkan ke tingkat sebelumnya.
Paroxetine dan Ketoconazole: Pemberian bersama paroxetine (20 mg sehari sekali selama 10 hari), inhibitor CYP2D6, dan ketoconazole (200 mg dua kali sehari) dengan beberapa dosis iloperidone (8 atau 12 mg dua kali sehari) untuk pasien dengan skizofrenia usia 18-65 tahun menghasilkan 1,4 peningkatan lipatan dalam konsentrasi mapan iloperidone dan metabolitnya P88 dan penurunan 1,4 kali lipat pada P95 di hadapan paroxetine. Jadi pemberian iloperidone dengan inhibitor dari kedua jalur metabolismenya tidak menambah efek dari kedua inhibitor yang diberikan sendirian. Dosis Iloperidone karenanya harus dikurangi sekitar setengah jika diberikan bersamaan dengan inhibitor CYP2D6 dan CYP3A4.
Potensi bagi FANAPT untuk Mempengaruhi Obat Lain
Studi in vitro dalam mikrosom hati manusia menunjukkan bahwa iloperidone tidak secara substansial menghambat metabolisme obat yang dimetabolisme oleh isozim sitokrom P450 berikut: CYP1A1, CYP1A2, CYP2A6, CYP2B6, CYP2C8, CYP2C9, atau CYP2E1. Lebih lanjut, penelitian in vitro dalam mikrosom hati manusia menunjukkan bahwa iloperidone tidak memiliki enzim yang menginduksi properti, khusus untuk isozim sitokrom P450 berikut: CYP1A2, CYP2C8, CYP2C9, CYP2C19, CYP3A4 dan CYP3A5.
Dekstrometorfan: Sebuah penelitian pada sukarelawan sehat menunjukkan bahwa perubahan farmakokinetik dextrometorfan (dosis 80 mg) ketika dosis 3 mg iloperidone diberikan bersama menghasilkan peningkatan total paparan 17% dan peningkatan 26% dalam konsentrasi plasma maksimum Cmax dari dekstrometorfan. Dengan demikian, interaksi antara iloperidone dan substrat CYP2D6 lainnya tidak mungkin.
Fluoxetine: Dosis tunggal iloperidone 3 mg tidak berpengaruh pada farmakokinetik fluoxetine (20 mg dua kali sehari).
Midazolam (substrat CYP 3A4 sensitif): Sebuah studi pada pasien dengan skizofrenia menunjukkan peningkatan kurang dari 50% dalam total midazolam pajanan pada keadaan stabil iloperidone (14 hari dosis oral hingga 10 mg iloperidone dua kali sehari) dan tidak berpengaruh pada midazolam C maks. Dengan demikian, interaksi antara iloperidone dan substrat CYP3A4 lainnya tidak mungkin.
Obat yang Memperpanjang Interval QT FANAPT tidak boleh digunakan dengan obat lain yang memperpanjang interval QT.
teratas
Gunakan Dalam Populasi Tertentu
Pendaftaran Kehamilan Kehamilan
Ada daftar pajanan kehamilan yang memantau hasil kehamilan pada wanita yang terpapar FANAPT selama kehamilan. Untuk informasi lebih lanjut, hubungi National Pregnancy Registry for Antipsikotik Atypical di 1-866-961-2388 atau kunjungi http://womensmentalhealth.org/clinical-and -research-program / kehamilan registry
Ringkasan Risiko
Neonatus yang ibunya terpapar obat antipsikotik, termasuk FANAPT, selama trimester ketiga kehamilan berisiko mengalami ekstrapiramidal dan / atau gejala penarikan setelah melahirkan. Data yang tersedia terbatas dengan FANAPT pada wanita hamil tidak cukup untuk menginformasikan risiko terkait obat untuk cacat lahir utama dan keguguran. Iloperidone tidak teratogenik ketika diberikan secara oral kepada tikus hamil selama organogenesis pada dosis hingga 26 kali dosis maksimum yang direkomendasikan manusia 24 mg / hari pada basis mg / m2. Namun, itu memperpanjang durasi kehamilan dan kelahiran, peningkatan kelahiran masih, kematian intrauterin awal, peningkatan kejadian keterlambatan perkembangan, dan penurunan kelangsungan hidup anak anjing post-partum. Iloperidone tidak teratogenik ketika diberikan secara oral kepada kelinci hamil selama organogenesis dengan dosis hingga 20 kali MRHD berdasarkan mg / m2. Namun, peningkatan kematian intrauterin dini dan penurunan viabilitas janin pada aterm pada dosis tertinggi yang juga merupakan dosis toksik maternal.
Risiko latar belakang cacat lahir utama dan keguguran untuk populasi yang ditunjukkan tidak diketahui. Pada populasi umum AS, risiko latar belakang yang diperkirakan dari cacat lahir utama dan keguguran pada kehamilan yang diakui secara klinis adalah masing-masing 2-4% dan 15-20%.
Pertimbangan Klinis
Reaksi Buruk Janin / Neonatal
Gejala ekstrapiramidal dan / atau penarikan, termasuk agitasi, hipertonia, hipotonia, tremor, somnolen, kesulitan pernapasan dan gangguan makan telah dilaporkan pada neonatus yang ibunya terpapar obat antipsikotik selama trimester ketiga kehamilan. Gejala-gejala ini bervariasi dalam keparahan. Beberapa neonatus pulih dalam beberapa jam atau hari tanpa perawatan khusus; yang lain membutuhkan rawat inap berkepanjangan. Pantau neonatus untuk gejala ekstrapiramidal dan / atau penarikan dan atasi gejala dengan tepat.
Data
Data Hewan
Dalam studi perkembangan embrio-janin, tikus hamil diberi 4, 16, atau 64 mg / kg / hari (1,6, 6,5, dan 26 kali lipat). dosis manusia maksimum yang direkomendasikan (MRHD) 24 mg / hari dengan basis mg / m2) iloperidone secara oral selama periode organogenesis. Dosis tertinggi menyebabkan peningkatan kematian intrauterin dini, penurunan berat dan panjang janin, penurunan osifikasi skelet janin, dan peningkatan insiden anomali skelet janin minor dan variasi; Dosis ini juga menyebabkan penurunan konsumsi makanan ibu dan penambahan berat badan.
Dalam studi pengembangan embrio-janin, kelinci hamil diberi 4, 10, atau 25 mg / kg / hari (3, 8, dan 20 kali MRHD berdasarkan mg / m2) iloperidone selama periode organogenesis. Dosis tertinggi menyebabkan peningkatan kematian intrauterin dini dan penurunan viabilitas janin saat aterm; dosis ini juga menyebabkan toksisitas ibu.
Dalam studi tambahan di mana tikus diberi iloperidone dengan dosis yang mirip dengan yang disebutkan di atas baik dari awal konsepsi atau dari hari ke 17 kehamilan dan berlanjut melalui penyapihan, efek reproduksi yang merugikan termasuk kehamilan yang berkepanjangan dan proses kelahiran, meningkat tingkat kelahiran mati, peningkatan kejadian variasi visceral janin, penurunan bobot janin dan anak anjing, dan penurunan anak post-partum bertahan hidup. Tidak ada efek obat pada perkembangan neurobehavioral atau reproduksi anak anjing yang masih hidup. Dosis tanpa efek berkisar antara 4 hingga 12 mg / kg kecuali untuk peningkatan tingkat kelahiran mati yang terjadi pada dosis terendah yang diuji 4 mg / kg, yaitu 1,6 kali MRHD berdasarkan mg / m2. Toksisitas ibu terlihat pada dosis yang lebih tinggi dalam penelitian ini.
The metabolit iloperidone P95, yang merupakan metabolit utama iloperidone yang bersirkulasi pada manusia tetapi tidak ada pada jumlah yang signifikan pada tikus, diberikan kepada tikus hamil selama periode organogenesis pada dosis oral 20, 80, atau 200 mg kg / hari. Tidak ada efek teratogenik yang terlihat. Pengerasan tulang yang terlambat terjadi pada semua dosis. Tidak ada toksisitas ibu yang signifikan yang diproduksi. Kadar P95 (AUC) plasma pada dosis tertinggi yang diuji adalah 2 kali lipat pada manusia yang menerima MRHD iloperidone.
Laktasi
Ringkasan Risiko
Tidak ada informasi mengenai keberadaan iloperidone atau metabolitnya dalam ASI efek iloperidon pada anak yang disusui, atau efek iloperidon pada ASI produksi. Iloperidone hadir dalam susu tikus. Karena potensi reaksi merugikan yang serius pada bayi yang disusui, anjurkan seorang wanita untuk tidak menyusui selama perawatan dengan FANAPT.
Data Pemindahan radioaktivitas ke dalam susu tikus menyusui diselidiki setelah dosis tunggal iloperidone [14C] pada 5 mg / kg. Konsentrasi radioaktivitas dalam susu pada 4 jam setelah dosis mendekati 10 kali lipat lebih besar daripada dalam plasma pada saat yang sama. Namun, pada 24 jam setelah pemberian dosis, konsentrasi radioaktivitas dalam susu turun ke nilai yang sedikit lebih rendah daripada plasma. Profil metabolisme dalam susu secara kualitatif mirip dengan dalam plasma.
Penggunaan Pediatrik Keamanan dan efektivitas pada pasien pediatrik dan remaja belum ditetapkan.
Penggunaan Geriatri
Studi klinis FANAPT dalam pengobatan skizofrenia tidak termasuk jumlah yang cukup pasien berusia 65 tahun ke atas untuk menentukan apakah mereka merespons secara berbeda atau tidak daripada orang dewasa yang lebih muda pasien. Dari 3.210 pasien yang diobati dengan FANAPT dalam uji coba pra pemasaran, 25 (0,5%) berusia ≥65 tahun dan tidak ada pasien yang berusia ≥75 tahun.
Pasien lanjut usia dengan psikosis terkait demensia yang diobati dengan FANAPT berada pada risiko kematian yang meningkat dibandingkan dengan plasebo. FANAPT tidak disetujui untuk perawatan pasien dengan psikosis terkait demensia.
Gangguan ginjal
Karena FANAPT sangat dimetabolisme, dengan kurang dari 1% obat yang diekskresikan tidak berubah, gangguan ginjal saja tidak mungkin memiliki dampak signifikan pada farmakokinetik FANAPT. Gangguan ginjal (bersihan kreatinin <30 mL / menit) memiliki efek minimal pada Cmax iloperidone (diberikan dalam dosis tunggal 3 mg) dan metabolitnya P88 dan P95 dalam salah satu dari 3 analit yang diukur. AUC0– increased meningkat sebesar 24%, menurun sebesar 6%, dan meningkat sebesar 52% untuk iloperidone, P88 dan P95, masing-masing, pada subjek dengan gangguan ginjal.
Ggn hati
Tidak diperlukan penyesuaian dosis untuk FANAPT pada pasien dengan gangguan hati ringan. Pasien dengan gangguan hati sedang mungkin membutuhkan pengurangan dosis. FANAPT tidak direkomendasikan untuk pasien dengan gangguan hati berat.
Pada subjek dewasa dengan gangguan hati ringan tidak ada perbedaan yang relevan dalam farmakokinetik iloperidone, P88 atau P95 (total atau tidak terikat) diamati dibandingkan dengan kontrol dewasa sehat. Pada subjek dengan gangguan hepar sedang, paparan bebas yang lebih tinggi (metabolit aktif) lebih tinggi (2 kali lipat) dan lebih bervariasi. diamati dibandingkan dengan kontrol sehat, sedangkan paparan iloperidone dan P95 umumnya serupa (kurang dari 50% perubahan dibandingkan dengan kontrol). Karena penelitian pada subyek gangguan hati berat belum dilakukan, FANAPT tidak direkomendasikan untuk pasien dengan gangguan hati berat.
Status Merokok
Berdasarkan penelitian in vitro yang menggunakan enzim hati manusia, FANAPT bukan substrat untuk CYP1A2; Oleh karena itu merokok seharusnya tidak berdampak pada farmakokinetik FANAPT.
Kehamilan
teratas
Penyalahgunaan dan Ketergantungan Narkoba
Zat Terkendali
FANAPT bukan zat yang dikendalikan.
Penyalahgunaan
FANAPT belum diteliti secara sistematis pada hewan atau manusia karena potensinya untuk pelecehan, toleransi, atau ketergantungan fisik. Sementara uji klinis tidak mengungkapkan kecenderungan perilaku mencari obat, pengamatan ini tidak sistematis dan tidak mungkin untuk memprediksi berdasarkan pengalaman ini sejauh mana obat aktif SSP, FANAPT, akan disalahgunakan, dialihkan, dan / atau disalahgunakan sekali dipasarkan. Akibatnya, pasien harus dievaluasi dengan cermat untuk riwayat penyalahgunaan obat, dan pasien tersebut harus diamati dengan cermat untuk tanda-tanda penyalahgunaan atau penyalahgunaan FANAPT (mis. pengembangan toleransi, peningkatan dosis, pencarian obat) tingkah laku).
teratas
Overdosis
Pengalaman Manusia
Dalam uji pra-pemasaran yang melibatkan lebih dari 3.210 pasien, overdosis FANAPT disengaja atau tidak disengaja didokumentasikan pada 8 pasien mulai dari 48 mg hingga 576 mg yang diminum sekaligus dan 292 mg diminum dalam 3 hari Titik. Tidak ada korban jiwa yang dilaporkan dari kasus ini. Konsumsi tunggal FANAPT terkonfirmasi terbesar adalah 576 mg; tidak ada efek fisik yang merugikan yang dicatat untuk pasien ini. Konsumsi FANAPT terbesar berikutnya adalah 438 mg selama periode 4 hari; gejala ekstrapiramidal dan interval QTc 507 msec dilaporkan untuk pasien ini tanpa sekuele jantung. Pasien ini melanjutkan pengobatan FANAPT selama 11 bulan tambahan.
Secara umum, tanda dan gejala yang dilaporkan adalah yang diakibatkan oleh berlebihannya efek farmakologis yang diketahui (misalnya, kantuk dan sedasi, takikardia, dan hipotensi) FANAPT.
Manajemen Overdosis
Tidak ada penangkal khusus untuk FANAPT. Karena itu langkah-langkah pendukung yang tepat harus dilembagakan. Dalam kasus overdosis akut, dokter harus membangun dan mempertahankan jalan napas dan memastikan oksigenasi dan ventilasi yang memadai. Bilas lambung (setelah intubasi, jika pasien tidak sadar) dan pemberian arang aktif bersama dengan pencahar harus dipertimbangkan. Kemungkinan perolehan, kejang atau reaksi distonik kepala dan leher setelah overdosis dapat menciptakan risiko aspirasi dengan emesis yang diinduksi. Pemantauan kardiovaskular harus dimulai segera dan harus mencakup pemantauan EKG terus menerus untuk mendeteksi kemungkinan aritmia. Jika terapi antiaritmia diberikan, disopyramide, procainamide dan quinidine tidak boleh digunakan, karena mereka memiliki potensi untuk efek pemanjangan QT yang mungkin aditif bagi FANAPT. Demikian pula, masuk akal untuk mengharapkan bahwa sifat alpha-blocking dari bretylium mungkin aditif bagi FANAPT, yang mengakibatkan hipotensi yang bermasalah. Hipotensi dan kolaps sirkulasi harus ditangani dengan tindakan yang sesuai seperti cairan intravena atau agen simpatomimetik (epinefrin dan dopamin tidak boleh digunakan, karena stimulasi beta dapat memperburuk hipotensi dalam pengaturan alpha yang diinduksi FANAPT blokade). Dalam kasus gejala ekstrapiramidal berat, obat antikolinergik harus diberikan. Tutup pengawasan medis harus dilanjutkan sampai pasien pulih.
teratas
Deskripsi
FANAPT adalah antipsikotik atipikal yang termasuk dalam kelas kimia turunan piperidinyl-benzisoxazole. Nama kimianya adalah 4 - - [3- [4- (6-Fluoro-1,2-benzisoxazol-3-yl) piperidino] propoxy] -3’-methoxyacetophenone. Formula molekulnya adalah C24H27FN2O4 dan berat molekulnya adalah 426,48. Rumus struktural adalah:
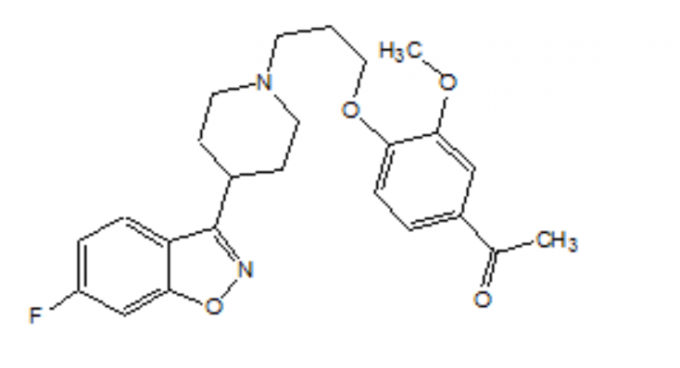
Iloperidone adalah bubuk kristal putih hingga putih. Ini praktis tidak larut dalam air, sangat sedikit larut dalam 0,1 N HCl dan bebas larut dalam kloroform, etanol, metanol, dan asetonitril.
Tablet FANAPT dimaksudkan hanya untuk pemberian oral. Setiap putaran, tanpa lapisan
tablet mengandung 1 mg, 2 mg, 4 mg, 6 mg, 8 mg, 10 mg, atau 12 mg iloperidone. Bahan aktif adalah: laktosa monohidrat, selulosa mikrokristalin, hidroksipropil metilselulosa, crospovidone, magnesium stearat, silikon koloid
dioksida, dan air murni (dihilangkan selama pemrosesan). Tablet-tablet itu berwarna putih, bulat, pipih, bermata miring dan diidentifikasi dengan logo "" diikat di satu sisi dan kekuatan tablet "1", "2", "4", "6", "8", "8", "10", atau "12" debossed di sisi lain.
teratas
Farmakologi Klinis
Mekanisme aksi
Mekanisme aksi iloperidone pada skizofrenia tidak diketahui. Namun kemanjuran iloperidone dapat dimediasi melalui kombinasi antagonisme dopamin tipe 2 (D2) dan serotonin tipe 2 (5-HT2).
Iloperidone membentuk metabolit aktif, P88, yang memiliki profil pengikatan reseptor in vitro mirip dengan obat induk.
Farmakodinamik
Iloperidone bertindak sebagai antagonis dengan afinitas tinggi (nM) yang mengikat serotonin 5-HT2A dopamin D2 dan Reseptor D3, dan reseptor norepinefrin NEα1 (nilai Ki dari 5,6, 6,3, 7,1, dan 0,36 nM, masing-masing). Iloperidone memiliki afinitas sedang untuk dopamin D4, dan serotonin 5-HT6 dan 5 -HT7 reseptor (nilai Ki 25, 43, dan 22, nM masing-masing), dan afinitas rendah untuk reseptor serotonin 5-HT1A, dopamin D1, dan histamin H1 (nilai Ki 168, 216 dan 437 nM, masing-masing). Iloperidone tidak memiliki afinitas yang cukup (Ki> 1000 nM) untuk reseptor muskarinik kolinergik. Afinitas metabolit iloperidon P88 umumnya sama dengan atau kurang dari senyawa induk, sedangkan metabolit P95 hanya menunjukkan afinitas untuk 5-HT2A (nilai Ki 3,91) dan reseptor NEα1A, NEα1B, NEα1D, dan NEα2C (nilai Ki 4,7, 2,7, 8,8 dan 4,7 nM masing-masing).
Farmakokinetik
Waktu paruh eliminasi rata-rata yang diamati untuk iloperidone, P88 dan P95 dalam CYP2D6 metabolizers ekstensif (EM) masing-masing 18, 26, dan 23 jam, dan pada metabolisme yang buruk (PM) masing-masing adalah 33, 37 dan 31 jam. Konsentrasi steady-state dicapai dalam 3-4 hari setelah pemberian dosis. Akumulasi Iloperidone dapat diprediksi dari farmakokinetik dosis tunggal. Farmakokinetik iloperidon lebih dari dosis proporsional. Eliminasi iloperidon terutama melalui metabolisme hati yang melibatkan 2 isozim P450, CYP2D6 dan CYP3A4.
Penyerapan: Iloperidone diserap dengan baik setelah pemberian tablet dengan konsentrasi plasma puncak terjadi dalam 2 hingga 4 jam; sedangkan bioavailabilitas relatif dari formulasi tablet dibandingkan dengan larutan oral adalah 96%. Pemberian iloperidone dengan makanan tinggi lemak standar tidak secara signifikan mempengaruhi Cmax atau AUC iloperidone, P88, atau P95, tetapi menunda Tmax sebesar 1 jam untuk iloperidone, 2 jam untuk P88 dan 6 jam untuk P95. FANAPT dapat diberikan tanpa memperhatikan makanan.
Distribusi: Iloperidone memiliki jarak bebas (clearance / bioavailabilitas) 47 hingga 102 L / jam, dengan volume distribusi yang jelas sebesar 1340-2800 L. Pada konsentrasi terapeutik, fraksi iloperidon yang tidak terikat dalam plasma adalah ~ 3% dan dari setiap metabolit (P88 dan P95) adalah ~ 8%.
Metabolisme dan Eliminasi: Iloperidone dimetabolisme terutama oleh 3 jalur biotransformasi: reduksi karbonil, hidroksilasi (dimediasi oleh CYP2D6) dan demetilasi O (dimediasi oleh CYP3A4). Ada 2 metabolit iloperidone dominan, P95 dan P88. The metabolit iloperidone P95 mewakili 47,9% dari AUC iloperidone dan metabolitnya dalam plasma pada kondisi mapan untuk metabolizers luas (EM) dan 25% untuk metabolizers buruk (PM). Akun metabolit P88 aktif masing-masing 19,5% dan 34,0% dari total paparan plasma pada EM dan PM.
Sekitar 7% -10% Kaukasia dan 3% -8% orang kulit hitam / Afrika Amerika tidak memiliki kapasitas untuk memetabolisme CYP2D6 substrat dan diklasifikasikan sebagai metabolisme buruk (PM), sedangkan sisanya bersifat menengah, luas atau ultrarapid metabolisme Pemberian bersama FANAPT dengan inhibitor kuat CYP2D6 seperti fluoxetine menghasilkan 2,3 kali lipat peningkatan paparan plasma iloperidone, dan karenanya setengah dari dosis FANAPT seharusnya dikelola.
Demikian pula, PMs dari CYP2D6 memiliki paparan iloperidone yang lebih tinggi dibandingkan dengan EM dan PMs harus memiliki dosis dikurangi setengahnya. Tes laboratorium tersedia untuk mengidentifikasi PMS CYP2D6.
Sebagian besar bahan radioaktif dipulihkan dalam urin (rata-rata 58,2% dan 45,1% dalam EM dan PM, masing-masing), dengan feses menyumbang 19,9% (EM) hingga 22,1% (PM) dari radioaktivitas dosis.
Interaksi Transporter: Iloperidone dan P88 bukan substrat P-gp dan iloperidone adalah inhibitor P-gp yang lemah.
teratas
Toksikologi Nonklinis
Karsinogenesis, Mutagenesis, Penurunan Kesuburan
Karsinogenesis: Studi karsinogenisitas seumur hidup dilakukan pada tikus CD-1 dan tikus Sprague Dawley. Iloperidone diberikan secara oral dengan dosis 2,5, 5.0 dan 10 mg / kg / hari untuk tikus CD-1 dan 4, 8, dan 16 mg / kg / hari untuk Tikus Sprague Dawley (0,5, 1,0 dan 2,0 kali dan 1,6, 3,2 dan 6,5 kali, masing-masing, MRHD 24 mg / hari pada mg / m2 dasar). Ada peningkatan insiden tumor kelenjar susu ganas pada tikus betina yang diobati dengan dosis terendah (2,5 mg / kg / hari) saja. Tidak ada peningkatan terkait neoplasia pada tikus.
Potensi karsinogenik dari metabolit iloperidon P95, yang merupakan metabolit utama iloperidone yang bersirkulasi pada manusia tetapi tidak ada pada jumlah yang signifikan pada tikus atau tikus, dinilai dalam studi karsinogenisitas seumur hidup pada tikus Wistar dengan dosis oral 25, 75 dan 200 mg / kg / hari pada laki-laki dan 50, 150, dan 250 (dikurangi dari 400) mg / kg / hari pada perempuan Perubahan neoplastik terkait obat terjadi pada laki-laki, di kelenjar hipofisis (pars distalis adenoma) pada semua dosis dan di pankreas (adenoma sel pulau) pada dosis tinggi. Tingkat plasma P95 (AUC) pada laki-laki pada dosis yang diuji (25, 75, dan 200 mg / kg / hari) masing-masing sekitar 0,4, 3, dan 23 kali, paparan manusia terhadap P95 pada MRHD iloperidone.
Mutagenesis: Iloperidone negatif pada tes Ames dan pada tes sumsum tulang tikus in vivo dan hati tikus. Iloperidone menginduksi aberasi kromosom pada sel Chinese Hamster Ovary (CHO) in vitro pada konsentrasi yang juga menyebabkan beberapa sitotoksisitas.
P95 metabolit iloperidone negatif pada uji Ames, uji penyimpangan kromosom V79, dan uji mikronukleus sumsum tulang tikus in vivo.
Penurunan Kesuburan: Iloperidone menurunkan kesuburan pada 12 dan 36 mg / kg dalam sebuah studi di mana tikus jantan dan betina diperlakukan. Dosis tanpa efek adalah 4 mg / kg, yaitu 1,6 kali MRHD 24 mg / hari dengan basis mg / m2.
teratas
Studi Klinis
Kemanjuran FANAPT dalam pengobatan skizofrenia didukung oleh 2 placebo dan uji coba jangka pendek (4 dan 6 minggu) yang dikontrol aktif dan terkontrol secara acak uji coba penarikan. Semua uji coba mendaftarkan pasien yang memenuhi kriteria DSM-III / IV untuk skizofrenia.
Tiga instrumen digunakan untuk menilai tanda dan gejala psikiatris dalam penelitian ini. Skala Sindrom Positif dan Negatif (PANSS) dan Skala Peringkat Psikiatri Singkat (BPRS) adalah inventori multi-item.
dari psikopatologi umum biasanya digunakan untuk mengevaluasi efek dari perawatan obat pada skizofrenia. Penilaian Clinical Global Impression (CGI) mencerminkan kesan seorang pengamat yang terampil, sepenuhnya akrab dengan manifestasi skizofrenia, tentang keadaan klinis keseluruhan pasien.
Sebuah percobaan 6 minggu, terkontrol plasebo (n = 706) melibatkan 2 rentang dosis fleksibel FANAPT (12-16 mg / hari atau 20-24 mg / hari) dibandingkan dengan plasebo dan kontrol aktif (risperidone). Untuk kelompok 12-16 mg / hari, jadwal titrasi FANAPT adalah 1 mg dua kali sehari pada Hari 1 dan 2, 2 mg dua kali sehari pada Hari 3 dan 4, 4 mg dua kali sehari pada Hari 5 dan 6, dan 6 mg dua kali setiap hari pada Hari 7. Untuk kelompok 20-24 mg / hari, jadwal titrasi FANAPT adalah 1 mg dua kali sehari pada Hari 1, 2 mg dua kali sehari pada Hari 2, 4 mg dua kali sehari pada Hari 3, 6 mg dua kali sehari pada Hari 4 dan 5, 8 mg dua kali sehari pada Hari 6, dan 10 mg dua kali sehari pada Hari 7. Titik akhir primer adalah perubahan dari awal pada skor total BPRS pada akhir pengobatan (Hari ke-42). FANAPT dosis 12-16 mg / hari dan 20-24 mg / hari lebih unggul dibandingkan plasebo pada skor total BPRS. Obat antipsikotik kontrol aktif tampaknya lebih unggul daripada FANAPT dalam percobaan ini dalam 2 yang pertama minggu, sebuah temuan yang sebagian dapat dijelaskan oleh titrasi yang lebih cepat yang dimungkinkan untuk itu obat. Pada pasien dalam penelitian ini yang tetap dalam pengobatan selama minimal 2 minggu, iloperidone tampaknya memiliki kemanjuran yang sebanding dengan kontrol aktif.
Sebuah 4 minggu, uji coba terkontrol plasebo (n = 604) melibatkan satu dosis tetap FANAPT (24 mg / hari) dibandingkan dengan plasebo dan kontrol aktif (ziprasidone). Jadwal titrasi untuk penelitian ini mirip dengan yang untuk studi 6 minggu. Penelitian ini melibatkan titrasi FANAPT mulai dari 1 mg dua kali sehari pada Hari 1 dan meningkat menjadi 2, 4, 6, 8, 10 dan 12 mg dua kali sehari pada Hari 2, 3, 4, 5, 6, dan 7. Titik akhir primer adalah perubahan dari baseline pada skor total PANSS pada akhir pengobatan (Hari 28). Dosis FANAPT 24 mg / hari lebih unggul dari plasebo dalam skor total PANSS. FANAPT tampaknya memiliki kemanjuran yang serupa dengan obat kontrol aktif yang juga membutuhkan titrasi lambat terhadap dosis target.
Dalam uji coba jangka panjang, pasien rawat jalan dewasa yang stabil secara klinis (n = 303) memenuhi kriteria DSM-IV untuk skizofrenia yang tetap stabil setelah 12 minggu pengobatan label terbuka dengan dosis fleksibel FANAPT (8 mg / hari - 24 mg / hari diberikan dalam dosis dua kali sehari) diacak ke plasebo atau dilanjutkan dosis FANAPT mereka saat ini (8 mg / hari - 24 mg / hari diberikan sebagai dosis dua kali sehari) untuk pengamatan kemungkinan kambuh selama kambuhan double-blind fase pencegahan. Stabilisasi selama fase label terbuka didefinisikan sebagai dosis FANAPT yang telah ditetapkan yang tidak berubah karena kemanjuran dalam 4 minggu sebelum pengacakan, memiliki skor CGI-Severity dari ≤4 dan total skor PANSS ≤70, skor ≤4 pada masing-masing item PANSS individu berikut (P1-delusi, P2-konseptual disorganization, Perilaku halusinasi P3, kecurigaan / penganiayaan P6, permusuhan P7, atau ketidak-kooperatif G8), dan tidak ada rawat inap atau peningkatan tingkat perawatan untuk diobati eksaserbasi. Relaps atau relaps yang akan datang selama fase pencegahan kambuhan double-blind didefinisikan sebagai salah satu berikut: rawat inap karena skizofrenia yang memburuk, peningkatan (memburuk) dari total skor PANSS ≥30%, CGI-
Skor perbaikan ≥6, pasien memiliki perilaku bunuh diri, pembunuhan, atau agresif, atau kebutuhan untuk obat antipsikotik lainnya.

Berdasarkan analisis sementara, komite pemantau data independen memutuskan penelitian harus dihentikan lebih awal karena bukti kemanjuran. Berdasarkan hasil dari analisis sementara, yang dikonfirmasi oleh dataset analisis akhir, pasien dirawat dengan FANAPT mengalami waktu yang signifikan secara statistik lebih lama untuk kambuh atau kambuh yang akan terjadi daripada pasien yang menerima plasebo. Gambar 1 menampilkan estimasi proporsi kumulatif pasien dengan kekambuhan atau kekambuhan yang akan datang berdasarkan set data akhir.
teratas
Bagaimana Disediakan / Penyimpanan dan Penanganan
Tablet FANAPT berwarna putih, bulat, dan diidentifikasi dengan logo yang dilepas di satu sisi dan kekuatan tablet "1", "2", "4", "6", "8", "10", atau "12" yang dilemparkan di sisi lain sisi. Tablet disediakan dalam kekuatan dan konfigurasi paket berikut:

Penyimpanan
Simpan tablet FANAPT pada suhu kamar terkontrol, 25 ° C (77 ° F); kunjungan diizinkan hingga 15 ° hingga 30 ° C (59 ° hingga 86 ° F) [Lihat USP Controlled Room Temperature]. Lindungi tablet FANAPT dari paparan cahaya dan kelembaban.
INFORMASI PENASIHAT PASIEN
Dokter disarankan untuk membahas masalah berikut dengan pasien yang mereka resepkan FANAPT:
Perpanjangan Interval QT
Pasien harus disarankan untuk berkonsultasi dengan dokter mereka segera jika mereka pingsan, kehilangan kesadaran atau jantung berdebar. Pasien harus dinasihati untuk tidak menggunakan FANAPT dengan obat lain yang menyebabkan perpanjangan interval QT. Pasien harus diberitahu untuk memberi tahu dokter bahwa mereka menggunakan FANAPT sebelum obat baru diminum.
Sindrom Maligna Neuroleptik
Pasien dan pengasuh harus diberi tahu bahwa suatu kompleks gejala yang fatal kadang-kadang disebut sebagai NMS telah dilaporkan dalam kaitannya dengan pemberian obat antipsikotik, termasuk FANAPT. Tanda dan gejala NMS termasuk hiperpireksia, kekakuan otot, perubahan status mental, dan bukti otonom
ketidakstabilan (nadi tidak teratur atau tekanan darah, takikardia, diaforesis, dan disritmia jantung).
Perubahan Metabolik
Pasien harus mewaspadai gejala hiperglikemia (gula darah tinggi) dan diabetes mellitus. Pasien yang didiagnosis menderita diabetes, mereka yang memiliki faktor risiko diabetes, atau mereka yang mengembangkannya gejala selama pengobatan harus dipantau glukosa darahnya di awal dan secara berkala selama pengobatan. Pasien harus diberitahu bahwa penambahan berat badan telah terjadi selama perawatan dengan FANAPT. Pemantauan klinis berat direkomendasikan.
Hipotensi ortostatik
Pasien harus diberitahu tentang risiko hipotensi ortostatik, terutama pada saat memulai pengobatan, memulai kembali pengobatan, atau meningkatkan dosis.
Gangguan dengan Kognitif dan Performa Motor
Karena FANAPT mungkin berpotensi mengganggu penilaian, berpikir, atau keterampilan motorik, pasien harus diwaspadai mengoperasikan mesin berbahaya, termasuk mobil, sampai mereka cukup yakin bahwa terapi FANAPT tidak memengaruhi mereka merugikan.
Kehamilan
Anjurkan pasien bahwa penggunaan Fanapt pada trimester ketiga dapat menyebabkan gejala ekstrapiramidal dan / atau penarikan pada neonatus. Anjurkan pasien untuk memberi tahu penyedia layanan kesehatan mereka dengan kehamilan yang diketahui atau diduga.
Daftar Kehamilan
Beri tahu pasien bahwa ada daftar pajanan kehamilan yang memantau hasil kehamilan pada wanita yang terpapar FANAPT selama kehamilan
Laktasi
Anjurkan wanita untuk tidak menyusui selama perawatan dengan FANAPT.
Obat bersamaan
Pasien harus disarankan untuk memberi tahu dokter mereka jika mereka menggunakan, atau berencana untuk mengambil, resep atau obat yang dijual bebas, karena ada potensi interaksi.
Alkohol
Pasien harus disarankan untuk menghindari alkohol saat mengambil FANAPT.
Paparan Panas dan Dehidrasi
Pasien harus diberitahu tentang perawatan yang tepat dalam menghindari overheating dan dehidrasi.
Didistribusikan oleh:
Vanda Pharmaceuticals Inc.
Washington, D.C. 20037 AS
Vanda dan Fanapt® adalah merek dagang terdaftar dari Vanda Pharmaceuticals Inc. di Amerika Serikat dan negara-negara lain.
kembali ke atas
Panduan Peresepan Fanapt (Iloperidone) (PDF)
Informasi dalam monograf ini tidak dimaksudkan untuk mencakup semua kemungkinan penggunaan, arahan, tindakan pencegahan, interaksi obat atau efek samping. Informasi ini digeneralisasi dan tidak dimaksudkan sebagai saran medis khusus. Jika Anda memiliki pertanyaan tentang obat-obatan yang Anda pakai atau ingin informasi lebih lanjut, tanyakan kepada dokter, apoteker, atau perawat Anda.
terakhir diperbarui 07/13
kembali ke: Halaman Utama Farmakologi Pengobatan Psikiatri



